C'est quoi de la silice
Pour répondre à cette question, il est important de définir en premier lieu ce qu’est le silicium. Cela dit, la silice est une forme de minerai provenant du silicium, d’où l’importance de le définir.
Le silicium, de son symbole Si, est un élément du tableau périodique de la catégorie des carbonés. Constituant environ 27,7% de la croute terrestre, le silicium tire son nom des termes latins « Silex » & « silicis », qui signifient respectueusement « silex » et « pierre dure ». Bien que le silicium pur est beaucoup trop réactif pour être retrouvé à son état pur de façon naturel, on le retrouve dans pratiquement tous les types de roches, le sable et les différents types de sols.
Les atomes de silicium sont essentiellement liés de manière covalente et sont très souvent entrelacés d’atomes d’oxygène. La disposition générale des atomes de silicium tend vers la formation des siloxanes. Ces siloxanes macromoléculaires ont généralement une masse assez importante pour être catégorisée comme étant des polymères. Lorsque les formations d’atomes de silicium ne présentent pas ces qualités, ils sont généralement sous forme aqueuse ou huileuse.
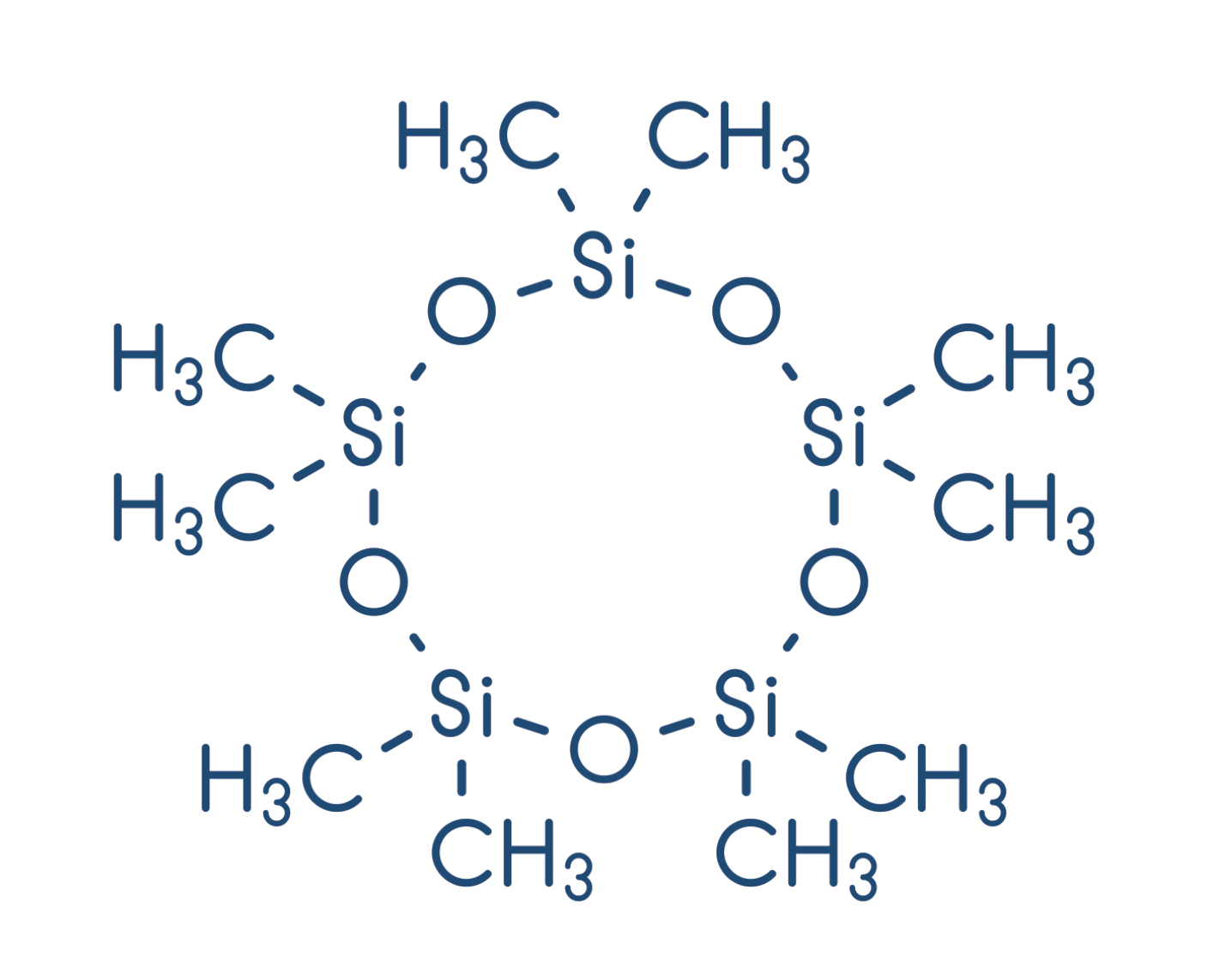
- Petite parenthèse, les siloxanes sont un groupe de composé organosilicié composé de squelettes Si – O – Si – O – Si avec des chaines latérales R qui s’attachent aux atomes de silicium. Par exemple, parmi les siloxanes les plus répandus, le polydiméthylsiloxane (PDMS) est le polymère le plus répandu dans l’industrie des silicones (tube de colle).
Bref, dans le secteur du traitement d’eau, c’est généralement sous ses formes minérales qu’on retrouve la présence de silicium.
Les formes minérales
Puisque le but de cet article n’est pas de présenter les dérivés minéraux du silicium, nous n’en aborderons que deux : les silicates et la silice.
Les silicates
Ils sont une famille de minéraux regroupant quelque 600 espèces minérales différentes. Leur point en commun est leur structure de base, soit une architecture atomique (SiO4)4-
Pour former un silicate, un anion de dioxyde de silicium situé au centre et entouré d’atomes d’oxygène s’associe à des cations métalliques (aluminium, magnésium, fer, etc.). Cet agencement permet la neutralité métallique des silicates.
Dans la catégorie des silicates, il existe plusieurs familles permettant leur identification. On peut penser aux nésosilicates, les sorosilicates, les cyclosilicates et bien plus.
La silice
Porteuse de plusieurs noms, la silice cristalline, la silice ou le dioxyde de silicium est un minerai communément retrouvé dans la nature. On la retrouve particulièrement dans les sables, les mortiers et le béton, mais on peut aussi la retrouver dans le verre, les poteries, la céramique, les briques et bien plus.
Comme son nom scientifique le laisse présager, la silice est constituée d’un atome de silicium et de deux atomes d’oxygène (SiO2). Comme pour les silicates, on retrouve plusieurs variétés de silice. Les trois variétés les plus répandues sont les quartz, les tridymites et les cristobalites.
Enfin, les minéraux purs de silice ont une apparence vitreuse et sont translucides. D’ailleurs, ils ne possèdent pas la qualité de conducteur.
La silice et l'eau
La présence de silice dans l’eau peut être causée par des activités humaines/industrielles puisque certains dérivés du silicium sont utilisés en tant que conditionneur, détergeant ou inhibiteur de corrosion
La silice peut aussi se propager de façon nature, et ce, principalement dû à l’érosion des sols et des minéraux. Cela se produit lorsque l’eau circule par-dessus ou au travers des différents types de sols.
- À des fins pratiques, nous n’élaborerons pas sur les différents types de sols, mais si le sujet vous intéresse, voici un article qui pourrait toucher votre curiosité: L'apport en eau minière : l'Impact des différents contaminants.
Lorsqu’elles proviennent de source naturelle, les traces de silice dans l’eau sont, majoritairement dû à l’hydrolyse des liaisons Si- O – Si. Lorsque cette réaction de dissolution a lieu, c’est sous forme d’acide silicique qu’on retrouvera la silice.
SiO2 + 2H2O -> SiO2 + H4SiO4
Typiquement, la concentration de silice dans les eaux naturelles tourne entre 5 et 25mg/L, mais il n’est pas anormal de recenser des concentrations dépassant les 100mg/L.
En solution, la silice est reconnue pour être très affectée par son environnement. Les facteurs comme la température, la cristallinité et le pH auront un impact sur le type de dégradation. En fonction de son environnement, trois produits dérivés de la silice peuvent se former.
- L’acide monosilicique
- L’acide polysilicique
- Particule de silice colloïdale
On distingue la silice en deux catégories lorsqu’elle est dissoute dans l’eau: la silice réactive et la silice non réactive.
La silice réactive
La silice réactive en est une dissoute dans l’eau, qui n’est pratiquement pas ionisée et qui n’a pas été polymérisée en une chaîne. Même si la silice réactive présente les caractéristiques d’un anion, elle est plutôt considérée comme étant partie des matières dissoutes totales (MDT). C’est cette donnée qui doit être considérée lorsqu’un programme de projection pour traitement à l’osmose inverse est créé.
La silice non réactive
On retrouve deux types de silices non réactives : les silices polymérisées et les silices colloïdales. Les silices colloïdales sont un mélange de siloxane (Si – O – Si) et silanol ( Si – OH). Leurs façons d’être font des silices colloïdales une substance très hydrophile et ayant la capacité de formée de maintes liaisons d’hydrogène. Ayant une taille frôlant les 0.008 micron, ce type de silice peut être extrait grâce à des osmoses inverses et on peut identifier sa présence grâce à un test SDI.
- Pour en apprendre plus sur le test SDI, visitez cet article: Qu'est-ce qu'un test SDI et comment le comprendre?
Même si les membranes osmotiques ont la capacité d’extraire ces amas colloïdaux, elles vont généralement avoir tendance à se boucher rapidement dû à la formation de silice sur l’extrémité de la membrane.
Lorsque la silice colloïdale n’est pas extraite adéquatement, si elle rentre en contact avec des équipements à haute température ou à haute pression, les colloïdes se brisent et peuvent s’accumuler sous une autre forme sur les parois des équipements.
Les risques associés à la présence de silice dans l'eau
Lorsque consommée dans l’eau, aucune preuve n’a démontré qu’il est néfaste ou dangereux pour la santé de consommer de l’eau possédant une concentration quelconque de silice. Évidemment, une concentration absurde de silice ou d’autres matières dissoutes dans l’eau peut être néfaste d’une manière ou d’une autre. En revanche, si cela est le cas, l’eau ne serait pas intéressante à la consommation (couleur, odeur, etc.).
- Petite précision, même si son ingestion n’est pas nocive pour la santé, il a été démontré que l’inhalation de la silice est la cause de maladie des poumons.
Les risques envers les équipements
La présence seule de silice n’a pas tendance à causer des problèmes aux équipements. Outre augmenter la difficulté de traitement de l’eau puisque la silice a tendance à encrasser les équipements de traitement d’eau, c’est ordinairement lorsque les systèmes sont opérés sous haute pression ou haute température que les problèmes surviennent.
C’est généralement sous forme de vapeur que la silice devient la plus problématique. Dans les bouilloires hautes pressions / haute température, la présence de silice peut causer des problèmes en avale lorsqu’elle se retrouve dans les vapeurs. Typiquement, plus la température/pression de la bouilloire est élevée, plus la concentration de silice dans la vapeur sera élevée. Lorsque cela survient, des dépôts se forment à l’intérieur du système ou sur les palmes des turbines et diminuent l’efficacité des équipements tout en augmentant les risques de bris ou d’accident.
Il est reconnu que pour éviter les risques et les complications reliés à la présence de silice ou de ses dérivés, dans une bouilloire haute pression/haute température, des concentrations de 0.02ppm sont le maximum à ne pas dépasser. Idéalement, il est conseillé d’être bien en dessous de cette limite. À titre d’exemple, un système de bouilloire évaporant 1000 tonnes d’eau à l’heure et ayant une concentration de 1ppm de silice, c’est 24kg de silice par jour qui s’accumulerait à l’intérieur du système.
Comment extraire la silice et ses dérivés?
Maintenant que l’on comprend comment et pourquoi la silice est problématique à l’égard des équipements industriels variés, attardons-nous à comprendre les techniques permettant son extraction.
Pour ce faire, il est important de préciser que les tactiques utilisées peuvent varier en fonction des besoins et des différentes situations. Par exemple, pour une bouilloire à moyenne pression avec une alimentation d’eau propre, le traitement sera plus simple que pour une même bouilloire avec une eau très contaminée.
L’ajout d’un système d’osmose inverse est très souvent la solution idéale pour la diminution de la silice et des autres contaminants se trouvant dans l’eau. En fonction de la qualité de l’eau d’alimentation et de sa concentration en silice, des étapes de préfiltration devront peut-être être installées. Différentes techniques de préfiltration peuvent être utilisées : adoucissement, coagulation, précipitation/agrégation, ultrafiltration, échangeur ionique ou filtre média.
Osmose inverse
Comme pour bien des utilisations, l’osmose inverse est très souvent le choix par excellence pour l’extraction des contaminants. C’est pareil dans le cas de la silice puisqu’on parle d’un taux de rejet des contaminants variant entre 95 et 99%[1]. La difficulté avec l’extraction de ce contaminant via osmose inverse est que la silice est la source principale d’encrassement des membranes osmotique.
Au fur et à mesure que l’osmose inverse traite l’eau, la concentration en silice augmente du côté du concentré[2]. À un certain niveau de saturation, les chances d’accumulation de dépôt de silice ou de silicates métalliques sur la surface augmentent de façon importante. Lorsqu’il y a accumulation, l’efficacité du traitement peut être affectée dus à une perte de perméabilité des membranes.
En plus de causer une détérioration des performances, l’accumulation de silice sur les membranes peut mener à d’autres problèmes. On peut penser à l’arrête complet du système pour cause de pression trop élevée ou à l’augmentation des coûts d’opération du système puisque l’énergie nécessaire pour effectuer le traitement est augmentée dus à l’encrassement des membranes.
Afin d’éviter ces problèmes, une étape de prétraitement peut être nécessaire ou l’ajustement du système d’osmose inverse peut suffire. Pour ce faire, on peut ajuster le taux de récupération de l’osmose inverse afin de réduire la saturation du concentré. En faisant cela, le pourcentage d’eau récupéré pour le traitement est diminué, ce qui augmente le coût de traitement par gallon, mais les chances de problèmes associés à la silice sont tout autant diminué.
Échange ionique à lit séparé
Les systèmes d’échange d’ions peuvent être très efficaces pour l’extraction de la silice. Avec la bonne disposition des résines, il est en effet possible d’extraire complètement la silice se retrouvant dans l’eau. C’est pourquoi ces systèmes sont utilisés pour le traitement de l’eau pour l’alimentation des bouilloires haute pression. Pour l’optimisation des coûts d’opération de ce type de système, les concentrations de silices dans l’eau ne devraient pas dépasser les 10 ppm.
Le principe de « lit séparé » consiste en deux réservoirs de résine qui sont installés en série. Pour l’extraction de la silice, le premier réservoir consiste en un lit de résine cationique qui doit être régénéré grâce à une solution acide. Le passage de la silice dans le réservoir cationique vient altérer sa composition et la « transforme » en acide silicique. Une fois cette conversion effectuée, l’acide silicique passe au travers du lit de résine anionique qui permettra l’extraction des acides. Entre les deux réservoirs de résines, il est commun de retrouver une unité de décarbonation afin de permettre l’extraction du gaz carbonique en forme aqueuse. Cette étape est importante puisque la résine anionique pourrait s’encrasser de CO2 avant de pouvoir extraire l’acide silicique se trouvant dans l’eau.
Les problèmes pouvant résulter d’une trop forte concentration en silice dans l’eau à traiter par un échangeur d’ions se résument à l’encrassement de la résine. Autrement dit, si la concentration de silice est trop élevée pour la taille de l’équipement, des accumulations peuvent se former et venir affecter l’efficacité du traitement. Pour remédier à cela, la régénération de résine doit toujours être effectuée adéquatement et des capteurs peuvent être installés sur le système.
Polissage
Puisque la silice est une molécule ionisée faiblement, durant les traitements comme l’échange ionique, les résidus d’autres molécules vont être extraits avant celle de la silice. C’est pourquoi il est fréquent de trouver des formes résiduelles de silice dans les eaux traitées par échange ionique ou osmose inverse.
Pour l’extraction complète des traces de silice, une étape de polissage est nécessaire. Le polissage consiste en un traitement additionnel de l’eau afin d’en extraire les particules les plus récalcitrantes ; comme la silice.
Pour ce type de contaminations, deux technologies sont réputées pour être efficaces et avantageuses : l’échangeur d’ions à lit mixte et l’électrodéionisation.
Échangeur d'ions à lit mixte
Le principe de cette technologie est exactement le même que celui de l’échangeur d’ions à lit séparé. La différence étant qu’ici, on retrouve un seul réservoir rempli d’un lit de résine mixte. Ce qui signifie que les résines anionique et cationique sont présentes dans le lit de résine.
Il est important de préciser que l’utilisation de cette technologie pour l’extraction de la silice ne peut être utilisée que pour le polissage de l’eau puisque des concentrations trop élevées de contaminants viendraient empêcher la captation des ions de silicium.
En revanche, si un échangeur d’ions à lit mixte est installé en avale d’un système d’osmose inverse ou d’un échangeur ionique à lit séparé, le point de contact entre les résines anionique et cationique permet d’aller retirer les résidus de silice ayant pu résister au traitement précédent.
Électrodéionisation (polissage)
Sans rentrer dans les détails du fonctionnement des modules EDI, ils opèrent grâce au même principe d’échange ionique que l’on retrouve dans les unités de traitement à lit de résine. Ce qui fait des modules EDI une technologie particulière est que le lit de résine est régénéré grâce à l’émission d’un courant électrique continue.
Puisque l’électrodéionisation fonctionne sous le même principe que l’échange ionique standard, elle a la capacité d’extraire toutes les traces de silices résiduelles dans l’eau.
Bien qu’ils soient très efficaces et peu coûteux à l’utilisation, ces systèmes sont très dispendieux à l’achat et ne sont utiles que pour le polissage de l’eau. L’avantage d’opter pour l’électrodéionisation est principalement associé au fait qu’aucune intervention n’est nécessaire pour fonctionner. Cela diminue ainsi les risques d’accident reliés à la manutention des produits chimiques servant à la régénération. Au niveau financier, les modules EDI sont généralement économiquement avantageux lorsque le débit d’eau se situe entre 20 gpm et 250 gpm.
Extraire la silice : chose possible
Comme on l’a vue plus haut, le silicium et ses dérivés peuvent causer des problèmes variés lorsqu’ils sont en présence de haute température ou de haute pression. Étant difficile à extraire, la présence de silice dans l’eau doit être abordée consciencieusement afin d’éviter de choisir une technologie de traitement non efficace ou peu optimisée en fonction de votre situation.
Bien qu’il existe d’autres méthodes permettant l’extraction de la silice, les technologies présenter sont celles présentant les meilleurs avantages et qui sont les plus versatiles.
Nous espérons que vos questions relativement au traitement de la silice ont été répondues. Vous avez d’autres questions ou problèmes, n’hésitez pas à communiquer avec nous.
D’ici là, nous vous invitons à consulter ces articles :
[1] Lorsque le taux de rejet d’une membrane osmotique est sous la barre des 95%, c’est généralement le moment de la changé.
[2] Dans une osmose inverse, le concentré fait référence au rejet suite au traitement. Autrement dit, l’eau pure traverse la membrane osmotique et le concentré est l’effluent ne pouvant pas être utilisé.